Enzymy
definice
Enzymy jsou chemické látky, které se nacházejí v celém těle. Uvádějí v těle do pohybu chemické reakce.
Dějiny
Slovo enzym byl vyroben uživatelem Wilhelm Friedrich Kühne 1878 a je odvozen z řeckého složeného slova enzymon, což znamená droždí nebo kynuté těsto. To si pak našlo cestu do mezinárodní vědy. The mezinárodní unie čisté aplikované chemie (IUPAC) a mezinárodní unie biochemie (IUBMB) společně vyvinuli nomenklaturu pro enzymy, která definuje zástupce této velké skupiny látek jako společnou skupinu. Pojmenování, které klasifikuje enzymy podle jejich úkolů, je důležité pro stanovení úkolů jednotlivých enzymů.
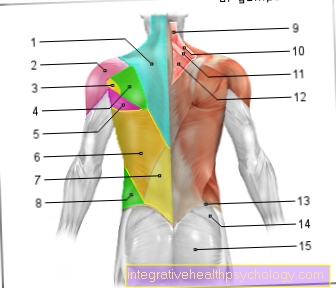
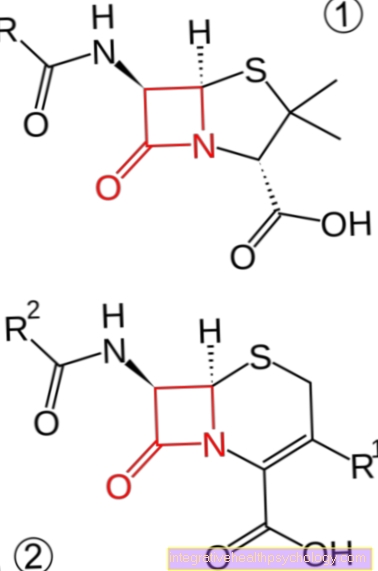
Ilustrace enzymů
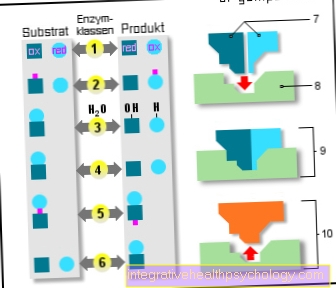
Enzymy
6 tříd enzymů:
- Oxidoreduktázy
(Oxidace / redukce) - Transferázy
(Přenos) - Hydrolázy
(Použití vody) - Lyázy
(Výstřih) - Izomerázy
(stejný empirický vzorec) - Ligázy
(Adiční reakce) - Substráty
- Aktivní centrum
- Enzym / substrát
komplex - Enzym / produkt
komplex
Přehled všechSnímky od Dr-Gumperta najdete na: lékařské ilustrace
Pojmenování
The Pojmenování enzym je zapnutý tři základní principy na základě. Názvy enzymů končící na –ase popisují několik enzymů v systému. Samotný název enzymu popisuje reakci, kterou enzym uvádí do pohybu (katalyzovaný). Název enzymu je také klasifikací enzymu. Navíc kódový systém, který Systém čísel ES, ve kterém jsou enzymy vyráběny pod číselným kódem čtyři čísla Může být nalezeno. První číslo označuje třídu enzymů. Seznamy všech detekovaných enzymů zajišťují rychlejší nalezení zadaného kódu enzymu. Ačkoli jsou kódy založeny na vlastnostech reakce, kterou enzym katalyzuje, v praxi se numerické kódy ukazují jako nepraktické. Systematické názvy založené na výše uvedených pravidlech se používají častěji. Problémy s nomenklaturou vznikají například s enzymy, které katalyzují několik reakcí. Proto pro ně někdy existuje několik jmen. Některé enzymy mají triviální názvy, které nenaznačují, že uvedená látka je enzym. Vzhledem k tomu, že názvy jsou tradičně široce používány, některé z nich byly zachovány.
Klasifikace podle funkce enzymu
Podle IUPAC a IUBMB jsou enzymy rozděleny do šesti tříd enzymů podle reakce, kterou uvedli do pohybu:
- Oxidoreduktázy
Oxidoreduktázy uvedly do pohybu redoxní reakce. Při této chemické reakci jsou elektrony přenášeny z jednoho reakčního partnera na druhého. Jedna látka uvolňuje elektrony (oxidace) a druhá látka přijímá elektrony (redukce).
Vzorec pro katalyzovanou reakci je A ^ + B? A + B.
Látka A uvolňuje elektron (?) A je oxidována, zatímco látka B tento elektron absorbuje a je redukována. Proto se redoxní reakce také nazývají redukčně-oxidační reakce.
Mnoho metabolických reakcí je redoxních reakcí. Oxygenázy přenášejí jeden nebo více atomů kyslíku na svůj substrát. - Transferázy
Transferázy přenášejí funkční skupinu z jednoho substrátu na druhý. Funkční skupiny jsou atomové skupiny v organických sloučeninách, které do značné míry určují vlastnosti látky a reakční chování. Chemické sloučeniny, které mají stejné funkční skupiny, jsou seskupeny do tříd látek kvůli jejich podobným vlastnostem. Funkční skupiny budou rozděleny podle toho, zda jsou heteroatomy nebo ne. Heteroatomy jsou všechny atomy v organických sloučeninách, které nejsou ani uhlíkem, ani vodíkem.
Např .: -OH -> hydroxylová skupina (alkoholy) - Hydrolázy
Hydrolázy štěpí vazby v reverzibilních reakcích pomocí vody. Estery, estery, peptidy, glykosidy, anhydridy kyselin nebo vazby C-C. Rovnovážná reakce je: A-B + H2O? A-H + B-OH.
Enzym, který patří do skupiny hydroláz, je např. Alfa galaktosidáza. - Lyázy
Lyázy, nazývané také syntázy, katalyzují štěpení komplexních produktů z jednoduchých substrátů bez odštěpování ATP. Reakční schéma je A-B → A + B.
ATP je adenosintrifosfát a nukleotid, který se skládá z trifosfátu nukleosidového adenosinu (a jako takový energeticky bohatý stavební blok RNA nukleové kyseliny). ATP je však hlavně univerzální formou okamžitě dostupné energie v každé buňce a zároveň důležitým regulátorem procesů dodávajících energii. V případě potřeby se ATP resyntetizuje z jiných zásob energie (kreatinfosfát, glykogen, mastné kyseliny). Molekula ATP se skládá z adeninového zbytku, cukrové ribózy a tří fosfátů (? To?) V esterových (?) Nebo anhydridových vazbách (? And?). - Izomerázy
Izomerázy urychlují chemickou přeměnu izomerů. Izomerismus je výskyt dvou nebo více chemických sloučenin s přesně stejnými atomy (stejný empirický vzorec) a molekulovými hmotnostmi, které se však liší ve spojení nebo v prostorovém uspořádání atomů. Odpovídající sloučeniny se nazývají izomery.
Tyto izomery se liší svými chemickými a / nebo fyzikálními vlastnostmi a často také svými biochemickými vlastnostmi. K izomerismu dochází primárně u organických sloučenin, ale také u (anorganických) koordinačních sloučenin. Izomerie je rozdělena do různých oblastí. - Ligázy
Ligázy katalyzují tvorbu látek, které jsou chemicky složitější než použité substráty, ale na rozdíl od lyáz jsou s štěpením ATP pouze enzymaticky účinné. Tvorba těchto látek proto vyžaduje energii, která se získává štěpením ATP.
Některé enzymy jsou schopné katalyzovat několik, někdy velmi odlišných reakcí. V takovém případě jsou zařazeny do několika tříd enzymů.
Také by vás mohly zajímat tyto články:
- Alfa-glukosidáza
- Lipáza
- Trypsin
Klasifikace podle struktury enzymu
Téměř všechny enzymy jsou proteiny a lze je klasifikovat na základě délky proteinového řetězce:
- Monomery
Enzymy, které se skládají pouze z jednoho proteinového řetězce - Oligomery
Enzymy, které se skládají z několika proteinových řetězců (monomerů) - Řetězy s více enzymy
Několik agregovaných enzymů, které spolupracují a navzájem se regulují. Tyto enzymové řetězce katalyzují následné kroky v metabolismu buňky.
Kromě toho existují jednotlivé proteinové řetězce, které obsahují několik enzymových aktivit; tyto se označují jako multifunkční enzymy.
Klasifikace podle kofaktorů
Jinou klasifikací je klasifikace podle zvážení kofaktorů. Kofaktory, koenzymy a ko-substráty jsou názvy pro různé klasifikace látek, které ovlivňují biochemické reakce prostřednictvím jejich interakce s enzymy.
Jsou brány v úvahu organické molekuly a ionty (většinou ionty kovů).
Čisté proteinové enzymy se skládají výhradně z proteinů a aktivní centrum je tvořeno pouze z aminokyselinových zbytků a peptidové kostry. Aminokyseliny jsou třídou organických sloučenin s alespoň jednou karboxylovou skupinou (-COOH) a jednou aminoskupinou (-NH2).
Holoenzymy se skládají z proteinové složky, apoenzymu a kofaktoru, molekuly s nízkou molekulovou hmotností (nikoli z proteinu). Oba jsou společně důležité pro funkci enzymu.
Koenzymy
Organické molekuly jako kofaktory se nazývají koenzymy. Pokud jsou kovalentně vázány na apoenzym, říká se jim protetické skupiny nebo ko-substráty. Protetická skupina označuje neproteinové složky pevně (většinou kovalentně) vázané na protein s katalytickým účinkem.
Kosubstráty jsou názvy pro různé klasifikace látek, které ovlivňují biochemické reakce prostřednictvím jejich interakce s enzymy. Jako biokatalyzátory molekuly urychlují reakce v organismech, enzymy urychlují biochemické reakce. Snižují aktivační energii, kterou je třeba překonat, aby bylo možné látku přeměnit.